L'IMAGING NELLA DIAGNOSI E FOLLOW-UP DELLE MALFORMAZIONI ANO-RETTALI
Macina F, Rossiello P, Mastronardi P*, Giangregorio F*, Martino F
U.O. di Radiologia - Ospedale pediatrico Giovanni XXIII - Bari
*U.O. di Chirurgia - Ospedale pediatrico Giovanni XXIII - Bari
INQUADRAMENTO CLINICO-PATOLOGICOUn ampio spettro di malformazioni ano-rettali si osserva approssimativamente in 1 caso su 5000 nati, con incidenza lievemente superiore nei maschi.
Un sistema di classificazione internazionale divide le malformazioni ano-rettali in quattro tipi: alte / intermedie / basse / miscellanea.
La mancata emissione di meconio e l'assenza dell'ano sono le più frequenti modalità di presentazione clinica nel neonato. L'attenta ispezione del perineo abitualmente è sufficiente ad identificare il tipo di anomalia ano-rettale. Una apertura perineale indica una lesione bassa e si verifica più frequentemente nelle femmine, nelle quali l'eventuale fistolizzazione si apre, spesso, in corrispondenza del fornice vaginale posteriore. Nei maschi, invece, la fistola si manifesta solo in concomitanza con la condizione di "ano imperforato coperto".
Le malformazioni ano-rettali possono presentarsi in "associazione" a difetti Vertebrali, Ano imperforato, fistola Tracheo-Esofagea, displasia del Radio e Renale, nota con l'acronimo di VATER.
Le anomalie vertebrali (tra le più frequenti l'agenesia sacrale, l'emivertebra, la fusione) sono presenti in più del 50% dei pazienti con malformazione alta e, meno frequentemente, nei pazienti con malformazioni basse.
Le più comuni anomalie del tratto urinario, presenti nel 25% delle atresie basse e nel 40% delle alte, includono il rene a ferro di cavallo, l'agenesia renale e l'ipoplasia, l'idronefrosi ed il reflusso vescica-ureterale.
Il diabete mellito è presente nel 16% circa dei pazienti affetti da agenesia sacrale.
L'anomalia del sacro si accompagna ad anomalie urologiche in oltre il 70% dei casi. Altre rare anomalie sono di immediato riscontro clinico, come la grave sindrome da regressione caudale, presente nei mostri sireniformi. In questi casi si verificano anche agenesia del tratto urinario e dei genitali interni, insieme alle anomalie del rachide lombo sacrale.
La triade di Currarino è riferita ad un complesso di anomalie congenite ("caudali") descritte da Kennedy nel 1926 e, poi, con maggiore precisione, da Currarino, nel 1981. l'anomalia include qualsivoglia tipo di malformazione ano-rettale, una massa pre-sacrale ed una anomalia del sacro. La massa pre-sacrale può essere rappresentata da un teratoma, un meningocele anteriore, una cisti enterica, ovvero una combinazione dei precedenti. Il sacro può presentarsi "segmentato" oppure avere un difetto a semiluna. L'eziologia non è chiara, ma può essere ricondotta a quella delle altre anomalie neuroenteriche riscontrabili in altre regioni anatomiche.
Lo studio radiologico della triade prevede un radiogramma diretto del rachide ed una valutazione RM del tratto rachideo lombo-sacrale. La scelta del trattamento terapeutico è in funzione del tipo di malformazione ano-rettale.
Le alterazioni "basse" sono trattate con l'anoplastica o la dilatazione della fistola; le intermedie e le alte rendono necessario un primo intervento colostomico ed un successivo completamento con anoplastica sagittale posteriore.
Una corretta distinzione tra forme alte e basse è di vitale importanza poiché una anoplastica estesa in un portatore di lesione alta ha elevata possibilità di complicarsi con ampie deformità chirurgiche iatrogene e con la possibile perdita della continenza fecale. Nella maggior parte dei casi i reperti clinici e radiologici sono sufficienti a porre una affidabile diagnosi pre-operatoria.
DIAGNOSTICA PER IMMAGINILa
radiografia convenzionale, sebbene prima dell'avvento delle grandi macchine costituisse la sola metodica impiegata nella differenziazione tra lesioni alte e basse in base alla posizione della tasca colica rispetto alla linea pubo-sacrococcigea, non offre da sola sufficiente affidabilità. Lo studio radiografico è rappresentato da un radiogramma antero-posteriore "in sospensione" e dal cosiddetto "invertogramma", costituito da un radiogramma diretto dell'addome in latero-laterale, a ginocchia e anche flesse, con il piccolo paziente sospeso in posizione anti-ortostatica. I radiogrammi (eseguiti almeno 24 ore dopo la nascita per consentire all'aria deglutita di progredire sino al tratto più distale del digerente) possono evidenziare, tipicamente, una occlusione intestinale distale (FIG. 1 A-B). Occasionalmente si può dimostrare la presenza di gas nella vescica (solo nei maschi), evocativa di una anomalia ano-rettale alta associata a comunicazione retto-uretrale o, meno frequentemente, retto-vescicale.
L'intrappolamento di meconio nell'intestino può dare luogo a calcificazioni qualora esista una fistola con il tratto urinario, cosa che si verifica abbastanza frequentemente sia nei maschi che nelle femmine.
Un uretere ectopico può drenare direttamente nel colon ed essere associato ad una malformazione ano-rettale con conseguente calcificazione meconiale. E' stata riportata in letteratura la calcificazione meconiale in assenza di fistole urinarie nella "prune belly sindrome" e la spiegazione più verosimile è quella della sola stasi. Le calcificazioni del contenuto colico, riportate nei pazienti affetti da malformazioni ano-rettali, trovano pressoché sempre la loro ragione di essere nella commistione delle urine al contenuto intestinale, per mezzo di una fistola vescico-enterica.
L'invertogramma in proiezione LL della pelvi è storicamente riconosciuto quale indagine in grado di dimostrare l'estensione longitudinale del colon. Tuttavia, nonostante l'impiego di vari reperi ossei o cutanei per indicare il livello della "fionda pubo-rettale", la tecnica è da considerarsi di limitata affidabilità in quanto gravata da potenziali artefatti in grado di impedire una corretta distinzione tra forme alte e forme basse. Infatti, l'"ispessimento" del meconio nel colon può impedire al gas intestinale di guadagnare la porzione distale dell'intestino; o, al contrario, una anomalia alta può essere scambiata per una bassa semplicemente in relazione al torchio addominale esercitato dal piccolo durante il pianto (l'incremento della pressione in addome si ripercuote sul pavimento pelvico e lo "disloca" rispetto ai reperi ossei della fionda pubo-rettale). E' tuttavia da tenere presente che l'esame radiografico consente di dimostrare la presenza delle eventuali malformazioni del rachide.
La
cistouretrografia minzionale (CUM) può consentire di identificare una fistola tra grosso intestino e vagina / vescica / uretra (FIG. 2). Nel maschio l'uretra, qualora esista un tragitto fistoloso retto-uretrale, presenta un caratteristico "inginocchiamento" posteriore (ed in detta situazione l'ipotesi di anomalia alta è la sola verosimile). Anomalie rare quali una fistola a decorso non abituale, una duplicazione uretrale e l'agenesia anale con fistola retto-bulbare sono facilmente dimostrabili in corso di CUM. L'agenesia anale associata ad una fistola retto-bulbare si verifica in meno del 2% dei piccoli con atresia anale. Se l'atresia anale non è associata ad un a fistola evidente ed è richiesta una valutazione pre-operatoria del colon, si può procedere ad una puntura percutanea della fossetta anale del perineo prima di procedere alla iniezione del m.d.c. (tutto sotto controllo scopico). L'impiego di un m.d.c. idrosolubile, oltre a dimostrare la posizione e morfologia del colon, consentirà anche, talvolta, di dimostrare un tragitto fistoloso. Non va dimenticata la possibilità, tramite la CUM, di studiare e classificare la presenza di un'eventuale patologia da reflusso vescico-ureterale.
L'
esame contrastografico dell'esofago potrà essere eseguito per dimostrare la presenza di un'atresia esofagea associata.
L'
indagine ecografica può consentire di misurare la distanza tra il tratto distale dell'intestino, disteso dal meconio, ed il perineo (se inferiore a 1,5 cm. deve essere considerata indicativa di una lesione bassa, mentre una "tasca colica" che termini cranialmente alla vescica indicherebbe una forma alta) (FIG. 3). Purtroppo rimangono, ad oggi, dubbi circa l'affidabilità della tecnica. Altri segni ecografici di lesione alta sono rappresentati da focolai intraluminali di iperecogenicità da riferire a gas nella vescica (analogo al reperto radiografico precedentemente descritto) ovvero a calcificazioni meconiali intraluminali. In aggiunta, l'ecografia ha il merito di dimostrare l'eventuale presenza di masse presacrali o di malformazioni renali e consente di porre sospetto di reflusso vescico-ureterale (eventualmente valutabile tramite cistosonografia).
La
risonanza magnetica e la
tomografia computerizzata possono risultare utili nella valutazione del complesso muscolare della fionda pubo-rettale nei piccoli affetti da anomalie congenite ano-rettali. La visualizzazione diretta della fionda pubo-rettale ed i suoi rapporti con il tratto distale del colon non solo sono un prezioso aiuto per il chirurgo, ma possono consentire di prevedere il grado di continenza che il piccolo paziente potrà raggiungere (FIG. 4). Se l'apparato muscolare non è presente non sarà possibile procedere con un intervento chirurgico di "pull-through" per ottenere la continenza. Lo studio in T1 sui tre piani con scansioni di 5 mm. contigue sono lo standard per le valutazioni RM. Il campo di vista deve includere il rachide lombo-sacrale, i reni e la pelvi (per consentire la dimostrazione di eventuali anomalie genito-urinarie e vertebrali associate). I muscoli pubo-rettali e lo sfintere anale esterno sono di facile dimostrazione su tutti i piani dello spazio con la RM. In caso di agenesia lombo-sacrale o di ipoplasia, il muscolo pubo-rettale e lo sfintere esterno saranno dimostrabili in una situazione anatomica "eccentrica".
Prima di procedere alla rimozione della colostomia può essere importante procedere con un "colostogramma distale" con m.d.c. idrosolubile, per rivalutare l'anatomia colica ed escludere possibili fistole (fino a quel momento misconosciute).
Dopo la definitiva procedura chirurgica di "pull-through" uno studio contrastografico, pur anche limitato al solo tratto distale del colon-sigma, può dimostrare prontamente l'eventuale deiscenza delle suture e, infine, l'incontinenza sfinteriale.
Qualora l'intestino non fosse stato correttamente "riposizionato" nel corso dell'intervento chirurgico, può residuare incontinenza fecale. In detta ipotesi uno studio RM consentirà la localizzazione dell'ansa intestinale rispetto al complesso sfinteriale.
La RM risulta utile anche nella dimostrazione di complicanze chirurgiche quali la impropria situazione anatomica del neoretto, l'improprio "trascinamento" di grasso mesenterico e l'impianto di cisti da ritenzione mucosa. Le sequenze sono analoghe a quelle dello studio pre-operatorio, mentre il campo di vista può essere limitato (ed escludere la colonna vertebrale o i reni, se precedentemente già esaminati). Alcuni autori suggeriscono di eseguire lo studio RM in tutti i pazienti candidati a ripetute procedure per persistente incontinenza.
BIBLIOGRAFIA - Anderson S, Savader B, Barnes J, Savader S. Enterolithiasis with imperforate anus. Report of two cases with sonographic demonstration and occurrence in a female. Pediatr Radiol 1988;18:130?3.
- Berdon WE, Baker DH, Santulli TV, et al. The radiologic evaluation of imperforate anus: an approach correlated with current surgical concepts. Radiology 1968;90:466?71.
- Berdon WE, Baker DH, Wigger HJ, et al. Calcified intraluminal meconium in newborn males with imperforate anus: enterolithiasis in the newborm. AJR 1975;125:449?55.
- Berdon WE, Hochberg B, Baker DH, et al. The association of lumbosacral spine and genitourinary anomalies with imperforate anus. AJR 1966;98:181?91.
- Cremin BJ. The radiological assessment of anorectal anomalies. Clin Radiol 1971;22:239?50.
- Currarino G, Cole D, Votteler T Triad of anorectal, sacral, and presacral anomalies. AJR 1981;137:395?8.
- Currarino G, Votteler T, Kirks DR. Anal agenesis with rectobulbar fistola. Radiology 1978;126:457?61.
- Donaldson JS, Black CT, Reynolds M, et al. Ultrasound of the distal pouch in infants with imperforate anus. J Pediatr Surg 1989;24:465?8.
- Duhamel B. From the mermaid to anal imperforation: the syndrome of caudal regression. Arch Dis Child 1961; 36:52?5.
- Felman AH, Walker RD, Donnelly WH, et al. Supralevator imperforate anus with unusual associated anomalies: colonic ureteral ectopy, intraluminal calcified meconium. Pediatr Radiol 1975;3:78?80.
- Gupta AK, Bhargava S, Rohtagi M. Anal agenesis with recto?bulbar fistola. Pediatr Radiol 1986;16:222?4.
- Kirks DR, Merten DF, Filston HC, et al. The Currarino triad: complex of anorectal malformafion, sacral bony abnormality, and presacral mass. Pediatr Radiol 1984; 14:220?5.
- Khoda E, Fujioka M, Ikawa H, Yokoyama J. Congenital anorectal anomaly: CT evaluation. Radiology 1985;I57: 349?52.
- Kurlander GJ. Roentgenology of imperforate anus. AJR 1967;100:190?201.
- Mezzacappa PM, Price AP, Haller JO. MR and CT demonstration of levator sling in congenital anorectal anomalies. J Comput Assist Tomogr 1987;11(2):273?5.
- Morgan CL, Grossman H, Novak R Imperforate anus and colon calcification in association with the prune belly syndrome. Pediatr Radiol 1978;7:19?21.
- Murugasu JJ. A new method of roentgenological demonstration of anorectal anomalies. Surgery 1970;68:706?12.
- Oppenheimer DA, Carroll BA, Shochat SJ. Sonography of imperforate anus. Radiology 1983;148:127?8.
- Pouillaude JM, Meyer P, Tran Minh U, et al. Enterolithiasis in two neonates with oesophageal and anorectal atresia. Pediatr Radiol 1987;17:419?21.
- Quan L, Smith DW The VATER association: vertebral defects, anal atresia, tracheoesophageal fistola with esophageal atresia, radial dysplasia. Birth Defects 1972; 8:75-8.
- Quan L, Smith DW. The VATER association: [V]ertebral defects, [A]nal atresia, [T?E] fistola with esophageal atresia, [R]adial and [R]enal dysplasia: a spectrum of associated defects. J Pediatr 1973;82:104?7,
- Santulli TU, Schullinger JN, Kiesewetter WB, et al. Imperforate anus: a survey from the members of the surgical section of the American Academy of Pediatrics. J Pediatr Surg 1971;6:484?7.
- Sato Y, Prìngle KC, Bergman RA, et al. Congenital anorectal anomalies: MR imaging. Radiology 1988; 168:157?62.
- Seibert JJ, Golladay ES. Clinical evaluation of imperforate anus: clue to type of anorectal anomaly. AJR 1979;133: 289?92.
- Selke AC, Cowley CE. Calcified intraluminal meconium in a female infant with imperforate anus. AJR 1978;130:786?8.
- Thompson W, Grossman H. The association of spinal and genitourinary abnormalities with low anorectal anomalies (imperforate anus) in female infants. Radiology 1974;113:693?8.
- Wagner ML, Harberg J, Kumar M, et al. The evaluation of imperforate anus utilizing percutaneous injection of water soluble iodide contrast media. Pediatr Radiol 1973;1:34?40.
DIDASCALIE
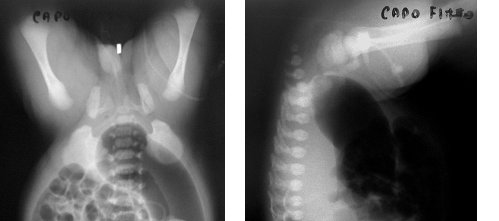
Fig. 1: L'invertogramma, in pr. AP (A) e LL (B), consente di dimostrare che il fondo del cul di sacco intestinale, ben disteso dal gas, si localizza ben al di sopra della linea pubo/sacro-coccigea (atresia "alta").
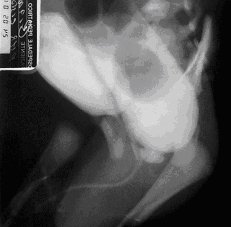
Fig. 2: CUM: atresia alta con fistola.
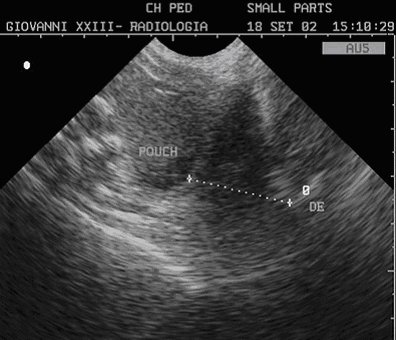
Fig.3: ETG scansione sagittale mediana: la distanza superiore a cm. 3, tra il cul di sacco ed il dito esploratore posto in fossetta anale, suggerisce la presenza di una atresia alta.
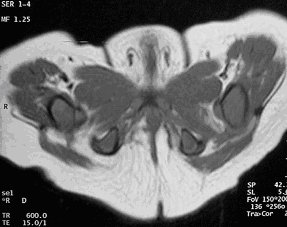
Fig. 4: RM SE T1 in scansione assiale: visualizzazione diretta della fionda pubo-rettale ed i suoi rapporti con il tratto distale del colon.